- О компании
- Решения и приложения
-
Направления деятельности
- Интернет-магазин
-
Медиатека
СтатьиСервис

10.06.2025
Сервисная сторона лаборатории: от инсталляции оборудования до постгарантийной поддержки
Интервью со специалистами технической поддержки Компании Хеликон.
СтатьиИнтервью
27.03.2024
Интервью Анатолия Смирнова телеканалу PROБизнес
«В любой биологической лаборатории в России есть что-то от нас».
- Новости
- Мероприятия
- Партнеры
О компании
Решения и приложения
- Главная страница
- Медиатека
- Информационные статьи
- Ребенок от трёх родителей: всё, что нужно знать о новом методе трёхстороннего ЭКО: поддержка Компании Хеликон
Медиатека
Ребенок от трёх родителей: всё, что нужно знать о новом методе трёхстороннего ЭКО
Оглавление:
•
В чём заключается метод трёхстороннего ЭКО?
•
Роль технологи в реальной жизни
•
Всё еще ранние дни
В мае 2023 года Британское управление по оплодотворению и эмбриологии человека (HFEA) подтвердило рождение не более пяти детей (точная цифра не разглашается в целях сохранения анонимности), зачатых с использованием новой экспериментальной технологии, объединяющей ДНК трёх человек – ДНК обоих родителей и митохондриальную ДНК донора. Об этом сообщила газета The Guardian. 1
Восемь лет назад Великобритания стала первой страной, законодательно регулирующей методы митохондриальной заместительной терапии 2, однако данная процедура всё ещё запрещена во многих государствах (в прошлом году Австралия стала второй страной, одобрившей её 3). В 2016 году врач из США объявил, что успешно провёл процедуру по предотвращению митохондриального заболевания у ребёнка в Мексике. 4 В результате трёхстороннего ЭКО также родились дети в Греции 5 и других странах.
На самом деле, ещё в 1990-х годах было задокументировано рождение младенцев в результате нового на тот момент метода, известного как ооплазматический перенос. Он был разработан в 1982 году и протестирован на животных, а затем и на людях. Изначально метод был предназначен для повышения жизнеспособности ооцитов и предотвращения бесплодия, а не митохондриальных болезней. 6
Ооплазматический перенос заключается в переносе небольшого количества цитоплазмы (включающей и митохондрии) из здоровой донорской яйцеклетки в яйцеклетку матери, которая затем оплодотворяется. Таким способом по официальным источникам в 1990-х и 2000-х было рождено не менее 30 детей. 7 Однако в 2002 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) решило регулировать эту процедуру из-за потенциального риска для здоровья детей. Дальнейшие испытания на людях в США были официально приостановлены и возобновились лишь недавно в Великобритании после долгих лет научных и этических дебатов.
В чём заключается метод трёхстороннего ЭКО?
Как известно, митохондрии содержат собственный генетический материал. Мутации в нём приводят к развитию митохондриальных заболеваний, таких как мышечная дистрофия, эпилепсия, проблемы с сердцем и умственная отсталость. Дети женщин-носителей причинных мутаций подвергаются высокому риску развития митохондриальных заболеваний, для большинства из которых в данный момент не существует специфического лечения.
Чтобы у семей появилась возможность рождения здоровых детей, были разработаны и одобрены два метода трёхстороннего ЭКО: перенос материнского веретена (MST) и пронуклеарный перенос (PNT). В обоих методах эмбрионы создаются с использованием ядерной ДНК родителей и здоровых донорских митохондрий. При этом из яйцеклетки донора удаляется собственный ядерный генетический материал и заменяется материнским.
В MST процесс переноса происходит до оплодотворения: ядерный генетический материал матери переносится в донорские яйцеклетки, которые затем оплодотворяются спермой для создания эмбрионов. В PNT яйцеклетки матери сначала оплодотворяются, и только после этого их ядерный генетический материал переносится в яйцеклетки донора (Рис.1). 8
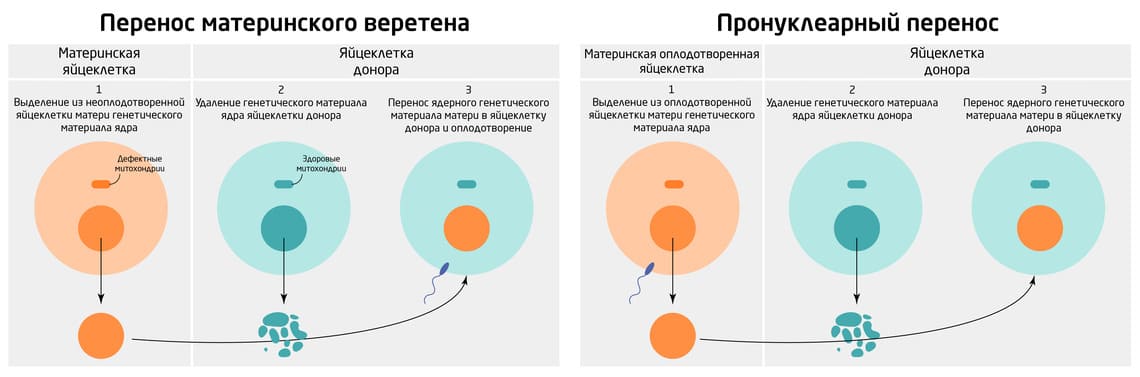
Рис. 1. Методы трехстороннего ЭКО.
Роль технологи в реальной жизни
Данная терапия даёт женщинам с тяжелыми наследственными митохондриальными заболеваниями возможность рождения здорового ребенка. При этом генетический материал донора составляет не больше 1%. 8
Эта технология не имеет ничего общего с так называемыми «дизайнерскими детьми», созданными с помощью генетического скрининга или генетической модификации. Хотя некоторые критики этого опасаются, учёные считают подобный исход маловероятным. Согласно действующим правилам, HFEA должен одобрять использование терапии в каждом конкретном случае. Чтобы получить разрешение на проведение процедуры, у женщины не должно быть других вариантов предотвращения передачи заболевания, таких как донорство яйцеклеток или скрининговые тесты (болезнь может не передаться ребенку, что и покажет тест).
Всё еще ранние дни
Новость действительно захватывающая, но учёные пока не понимают, действительно ли этот метод безопасен и эффективен. Всё еще есть вопросы и этические соображения. Поэтому крайне важно наблюдать за развитием младенцев, чтобы понять, остаются ли уровни перенесённых мутантных митохондрий стабильными с течением времени и существует ли риск развития проблем с возрастом.
Исследования показали, что небольшое количество дефектных митохондрий неизбежно переносится в яйцеклетку донора вместе с ядерным материалом. Такие митохондрии могут размножаться, вытесняя митохондрии донора. Это явление, которое учёные называют «реверсией», может вызвать у ребёнка генетическое заболевание. 9, 10 Причины и вероятность такого исхода пока не известны.
Митохондриальный перенос был встречен как с восторгом, так и с критикой, поскольку последствия этой революционной и многообещающей терапии до конца не изучены. Необходимы дальнейшие наблюдения и исследования — только строгий контроль навигации по методу трёхстороннего ЭКО позволит обеспечить благополучие будущих поколений, рождённых таким способом.
Литература
1. First UK baby with DNA from three people born after new IVF procedure. The Guardian, 2023.
2. MPs vote in favour of 'three-person embryo' law. The Guardian, 2015.
3. Australia Moves Ahead Cautiously With '3-Parent IVF'. Wired, 2022.
4. Reardon S. ‘Three-parent baby’ claim raises hopes — and ethical concerns. Nature, 2016.
5. ‘Three-person’ baby boy born in Greece. BBC, 2019.
6. Darbandi S. et al. Ooplasmic transfer in human oocytes: efficacy and concerns in assisted reproduction. Reproductive Biology and Endocrinology, 2017.
7. Barritt J.A. et al. Cytoplasmic transfer in assisted reproduction. Human Reproduction Update, 2001.
8. Mitochondrial donation treatment. Human Fertilisation & Embryology Authority.
9. Kang E. et al. Mitochondrial replacement in human oocytes carrying pathogenic mitochondrial DNA mutations. Nature, 2016.
10. Costa-Borges N. et al. First pilot study of maternal spindle transfer for the treatment of repeated in vitro fertilization failures in couples with idiopathic infertility. Fertility and Sterility, 2023.




.jpg)