Медиатека
Микробиом и метаболом: как кишечные бактерии влияют на метаболизм мышей?
В желудочно-кишечном тракте (ЖКТ) человека живёт около 100 триллионов бактерий – от 300 до 500 видов. 1, 2 Большая часть из них – «хорошие». Что это значит? «Хорошие» бактерии, комменсальные, живут в симбиозе с организмом человека, не только не причиняя ему вреда, но и принося пользу. Другие бактерии абсолютно безвредны в норме, но при некоторых условиях могут вызывать инфекционные заболевания. Их называют условно-патогенными. 3
Комменсалы регулируют баланс микрофлоры ЖКТ, влияют на иммунитет, мозг, абсорбцию питательных веществ эпителиальными клетками кишечника и даже поведение хозяина. Эти физиологические эффекты достигаются за счёт метаболитов, которые образуются в результате жизнедеятельности кишечных бактерий и проникают в ткани и системный кровоток (например, короткоцепочечные жирные кислоты – продукты распада неперевариваемых сложных углеводов и белков, продукты метаболизма триптофана, лактат, инозин и желчные кислоты). Исследования на мышах показали, что состав микробиоты кишечника влияет на множество биохимических процессов практически во всех органах. 4, 5 Например, на метаболизм желчных кислот и антиоксидантов (получаемая из триптофана индол-3-пропионовая кислота, которая обладает нейропротекторным и противовоспалительным действием).
Основные функции кишечной микрофлоры (рис. 1) 1:
- Метаболическая.
- Энергетический обмен.
- Образование короткоцепочечных жирных кислот.
- Синтез незаменимых аминокислот (аргинин, глютамин).
- Синтез витаминов (витамин К, фолиевая кислота, витамин В12).
- Метаболизма лекарств (например, образование 5-аминосалициловой кислоты из сульфасалазина).
- Деконъюгация желчных кислот (гидролиз амидной связи между глицином или таурином, конъюгированным со стероидным ядром). 6
- Предотвращение роста патогенной микрофлоры.
- Иммунная регуляция.
- Стимуляция выработки иммуноглобулина А.
- Стимуляция высвобождения противовоспалительных цитокинов и подавление активности провоспалительных цитокинов.
- Активация Т-клеток.
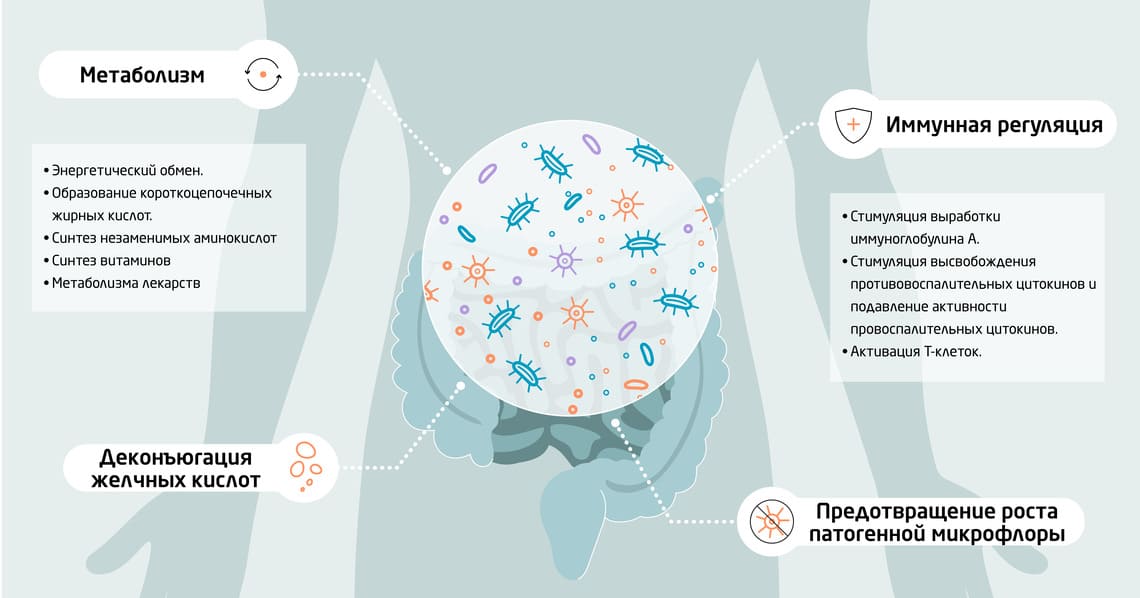 Рис. 1. Основные функции микрофлоры ЖКТ.
Рис. 1. Основные функции микрофлоры ЖКТ.
Авторам новой работы, опубликованной в журнале Nature Communications, удалось показать, что не только состав микрофлоры кишечника, но и эффекты продуктов метаболизма зависят от множества факторов, включая пол и возраст, отдел ЖКТ, питание и даже условия содержания животных. 7 Учёные использовали 3 группы мышей линии C57BL/6 в возрасте 3, 8 и 12 недель.
Животные 1-ой группы были полностью лишены бактериальной микрофлоры (germ-free, GF), животные 2-ой группы – только патогенной микрофлоры (specific pathogen-free, SPF), а животные 3-ей группы (гнотобиотические) были колонизированы 12 видами комменсальных бактерий (OMM12), которые относятся к 5 основным типам прокариот, обитающих в ЖКТ мышей (Bacteroidota, Bacillota, Pseudomonadota, Actinomycetota и Verrucomicrobiota).
Состав и уровень метаболитов определяли в печени, селезёнке и кишечнике с помощью жидкостной хроматографии и масс-спектрометрии. Ткани предварительно гомогенизировали и центрифугировали, а затем помещали в 96-луночную плашку для последующего анализа. Метаболиты разделяли при скорости потока 600 мкл/мин с использованием 2-х растворителей (растворитель A, 20 мМ формиат аммония, pH 3.0 и растворитель B, ацетонитрил с 0.1% муравьиной кислоты). Затем проводили масс-спектрометрию в режиме негативного полного сканирования с разрешением 240 000 сканирований в диапазоне 50–750 m/z (отношение массы к заряду). Этот эксперимент можно воспроизвести с помощью системы ультравысокоэффективной жидкостной хроматографии/масс-спектрометрии на базе тройного квадруполя HELICON 5210.
Экстракцию и очистку ДНК бактерий из кишечного содержимого проводили с помощью набора для выделения ДНК. Область V4 гена 16S рРНК амплифицировали с использованием праймеров, содержащих баркоды исследуемых штаммов бактерий, и полимеразы KAPA HiFi с последующим циклом. Полученные индивидуальные библиотеки объединяли в единый ампликон и секвенировали.
Результаты исследования продемонстрировали тесное двустороннее взаимодействие между организмом хозяина и жизнедеятельностью бактерий. Как и ожидалось, кишечная микробиота оказывала наибольшее влияние на состав метаболитов (метаболом) в нижних отделах ЖКТ – слепой и толстой кишке. Бактерии типа OMM12 влияли на содержание 49% и 54% метаболитов, а бактерии микрофлоры SPF – 52% и 62% метаболитов в слепой и толстой кишке, соответственно (рис. 2). Это согласуется с данными предыдущих исследований, которые неоднократно показывали, что именно эти отделы кишечника наиболее плотно колонизированы бактериями у всех млекопитающих, поэтому микробиологический состав в этих областях вносит наибольший вклад в метаболизм организма хозяина.
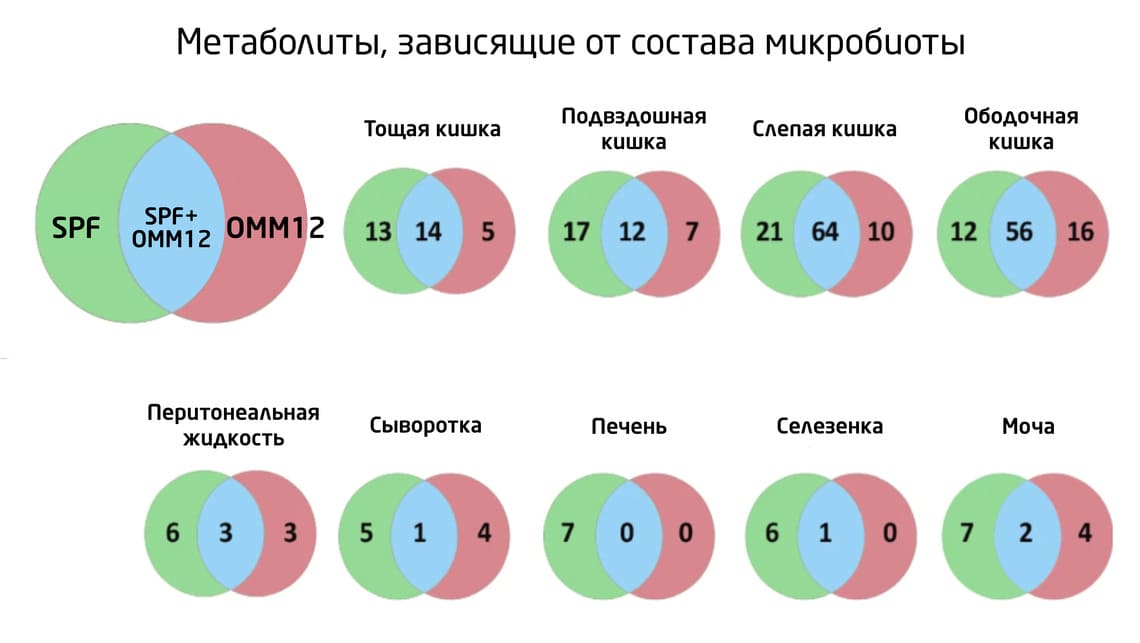 Рис. 2. Распределение количества метаболитов в разных отделах: OMM12 относительно GF (красный), SPF относительно GF (зелёный), а также OMM12 SPF относительно GF (синий).
7
Рис. 2. Распределение количества метаболитов в разных отделах: OMM12 относительно GF (красный), SPF относительно GF (зелёный), а также OMM12 SPF относительно GF (синий).
7
Однако данный эффект не ограничивался только нижними отделами ЖКТ – колонизация также регулировала содержание метаболитов в нижних и средних отделах ЖКТ. При этом не только наличие, но и состав микрофлоры оказывал влияние на метаболизм органических соединений. Например, в нижних отделах ЖКТ аллантоин утилизировался только микробиотой SPF, в то время как одноосновная мононенасыщенная тригидроксимонокарбоновая кислота шикимат, необходимая для синтеза ароматических аминокислот и фолиевой кислоты, а также трисахарид рафиноза, состоящий из галактозы, глюкозы и фруктозы, активно использовались как микробиотой OMM12, так и микробиотой SPF.
Интересно, что фермент, необходимый для расщепления рафинозы, – α-галактозидаза – не содержится в ЖКТ млекопитающих с однокамерным желудком. Значит, расщеплять этот трисахарид могут только бактерии. Оба типа микробиоты также способны продуцировать никотиновую кислоту – витамин группы B и предшественник никотинамидадениндинуклеотида.
Результаты исследования ещё раз подтвердили, что бактериальная флора играет важнейшую роль в метаболизме и регуляции биодоступности желчных кислот. Однако эти процессы зависели и от состава микрофлоры. Например, холат (остаток холевой кислоты) вырабатывался у всех мышей с бактериальной микрофлорой, в то время как таурохолат, который образуется при конъюгации холата с таурином в печени, присутствовал только у мышей с SPF (оба соединения являются первичными желчными кислотами.). Это значит, что у бактериальной флоры OMM12 недостаточно ферментативной активности для этого биохимического превращения. В верхних отделах ЖКТ мышей, лишённых микрофлоры, в целом содержалось гораздо меньше холевой кислоты (одна из желчных кислот), жирных кислот и нуклеозидов, чем у мышей других групп, но было больше сахаров.
Уровень метаболитов в ЖКТ мышей также зависел от возраста и пола животных. Как и микробиом, метаболом больше всего менялся с возрастом в нижних отделах кишечника, что ещё раз указывает на связь между деятельностью бактерий и метаболизмом. Например, микрофлора кишечника играет важную роль в поддержании стабильной концентрации некоторых органических биологически активных соединений, таких как орнитин, гистидин, уридин и глутамин. У животных, лишённых микрофлоры, их концентрация повышалась с возрастом (рис. 3).
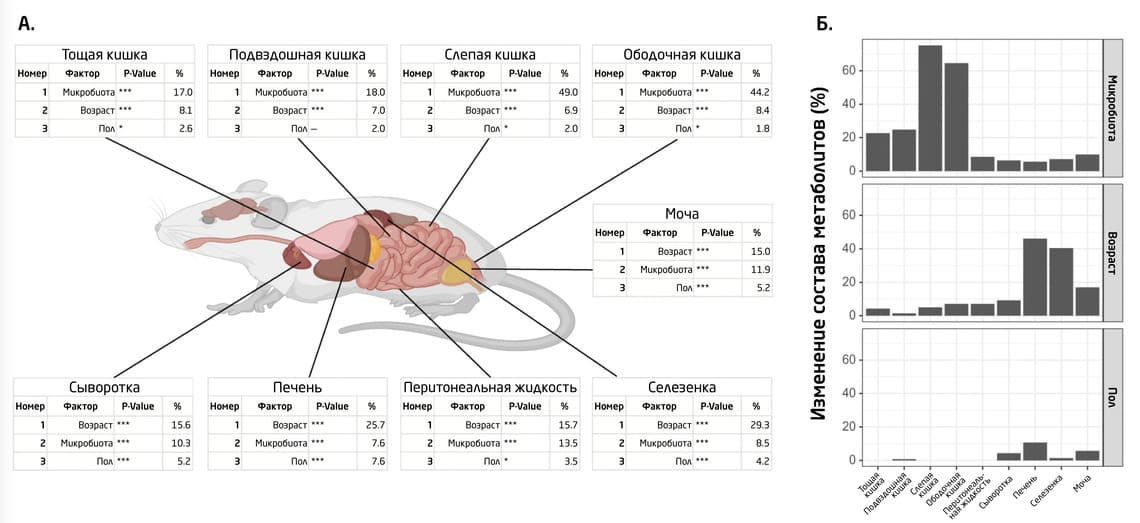 Рис. 3. (А) Процентное соотношение влияния микробиоты, возраста и пола на метаболиты. В сыворотке, моче и перитонеальной жидкости влияние микробиоты и возраста одинаково, тогда как в печени и селезёнке возраст оказывает большее влияние, чем микробиом. (Б) Изменение состава метаболитов под влиянием микробиома, возраста и пола.
7
Рис. 3. (А) Процентное соотношение влияния микробиоты, возраста и пола на метаболиты. В сыворотке, моче и перитонеальной жидкости влияние микробиоты и возраста одинаково, тогда как в печени и селезёнке возраст оказывает большее влияние, чем микробиом. (Б) Изменение состава метаболитов под влиянием микробиома, возраста и пола.
7
Наконец, микробиота может быть одним из факторов, влияющих на гендерные различия в устойчивости к заболеваниям и иммунных функциях. У самцов, колонизированных микробиотой SPF, в слепой и толстой кишке был выше уровень индолацетата – соединения, способного снижать уровень воспаления, регулировать активность макрофагов и индуцированный цитокинами липогенез в гепатоцитах. У самцов и самок были также обнаружены различия в метаболизме пуринов, опосредованном микробиотой. Например, у самцов в нижних отделах ЖКТ был выше уровень инозина, а у самок – его метаболического предшественника аденина (превращается в инозин через аденозин или инозинмонофосфат). Инозин известен своим влиянием на транскрипцию и способностью регулировать противоопухолевую активность Т-клеток. Учёные предполагают, что эти различия могут быть связаны с действием половых гормонов.
Трудность изучения обширных физиологических эффектов бактериальных метаболитов заключается в невозможности отделить метаболические пути кишечной микрофлоры и организма хозяина. И, хотя за последние годы наука продвинулась в понимании этих механизмов, учёные считают, что им известна лишь вершина айсберга. 7 Результаты работы показывают, что микробиота не просто живёт и питается за счёт организма животного, но и меняется вместе с ним, например, с возрастом или в ответ на гормональные изменения. Эти данные открывают новые горизонты для будущих исследований. Одна из интересных тем для изучения – можно ли «настраивать» или менять микрофлору так, чтобы она приносила максимальную пользу?
Литература
1. Quigley Eamonn M.M. Gut bacteria in health and disease. Gastroenterology & Hepatology, 2013.
2. Guinane C.M., Paul D.C. Role of the gut microbiota in health and chronic gastrointestinal disease: understanding a hidden metabolic organ. Therapeutic Advances in Gastroenterology, 2013.
3. Haque S.Z., Mainul H. The ecological community of commensal, symbiotic, and pathogenic gastrointestinal microorganisms – an appraisal. Clinical and Experimental Gastroenterology, 2017.
4. Wikoff W.R. et al. Metabolomics analysis reveals large effects of gut microflora on mammalian blood metabolites. Proceedings of the National Academy of Sciences USA, 2009.
5. Kim Ch.-Su. Gut microbiota indole-3-propionic acid mediates neuroprotective effect of probiotic consumption in healthy elderly: A randomized, double-blind, placebo-controlled, multicenter trial and in vitro study. Clinical Nutrition (Edinburgh, Scotland), 2023.
6. Urdaneta V. Interactions between Bacteria and Bile Salts in the Gastrointestinal and Hepatobiliary Tracts. Frontiers in medicine, 2017.
7. Brown K. et al. Microbiota alters the metabolome in an age- and sex- dependent manner in mice. Nature Communications, 2023.




.jpg)