Медиатека
Эволюция Chlamydiae: от свободноживущих форм к эндосимбионтам
Ежегодно выявляется до 130 млн случаев инфицирования бактериями типа Chlamydiae 1. В отличие от других свободноживущих представителей надтипа Planctomycetes–Verrucomicrobia–Chlamydiae (PVC; эволюционно отделились от родственных групп ~1-2 млрд лет назад 2), современный тип Chlamydiae представлен облигатными эндосимбионтами животных и простейших. Они могут выполнять роль патогенов или приносить пользу хозяину (мутуализм).
Хламидии семейства Parachlamydiaceae защищают простейших от вирусов и других бактерий (например, Legionella pneumophila 3), а потому имеют больше генов и более адаптивную систему энергетического обмена по сравнению с патогенами животных, Chlamydiaceae 4, 5. Представители семейства Chlamydia, наоборот, являются социально значимыми патогенами. Chlamydia trachomatis вызывает глазные заболевания (трахома) и заболевания, передающиеся половым путём, а Chlamydia pneumoniae является возбудителем острых респираторных инфекций у человека и животных 1.
В связи со сложностью в культивировании наличие хламидийной инфекции в клиническом материале определяют с помощью полимеразной цепной реакции (ПЦР). Для усиления сигнала, повышения специфичности и объективности интерпретации результатов применяют также ПЦР с гибридизационно-флуоресцентной детекцией в режиме реального времени. При выборе тест-системы для молекулярной диагностики ключевым критерием является чувствительность реагентов. Среди наборов, соответствующих требуемым критериям, можно назвать тест-системы российского производства «АмплиСенс®».
На вопрос, как и когда свободноживущие микроорганизмы стали эндосимбионтами, ответили авторы новой работы в журнале Nature Microbiology 5. На основе данных о различиях в так называемых маркерных генах (single-copy marker genes) учёные смоделировали эволюцию 180 представителей надтипа PVC, включая 91 из группы Chlamydiae.
Маркерные гены – это ортологичные гены (гомологичные гены филогенетически родственных организмов), которые участвуют в регуляции жизненно важных процессов в клетке 6. Яркий пример – ген 16S рибосомальной РНК у прокариот и 18S у эукариот 7, 8.
Реконструкция генетической последовательности практически 12 тыс. семейств генов позволила найти последнего общего с другими типами PVC предка Chlamydiae – подвижную факультативно анаэробную бактерию. Большинство из приобретённых генов (401 из 1118) было связано с метаболизмом, например, синтезом и деградацией гликогена. Гены, необходимые для взаимодействия с хозяином и смены фаз жизненного цикла, были унаследованы от более ранних предковых форм (Рис.1).
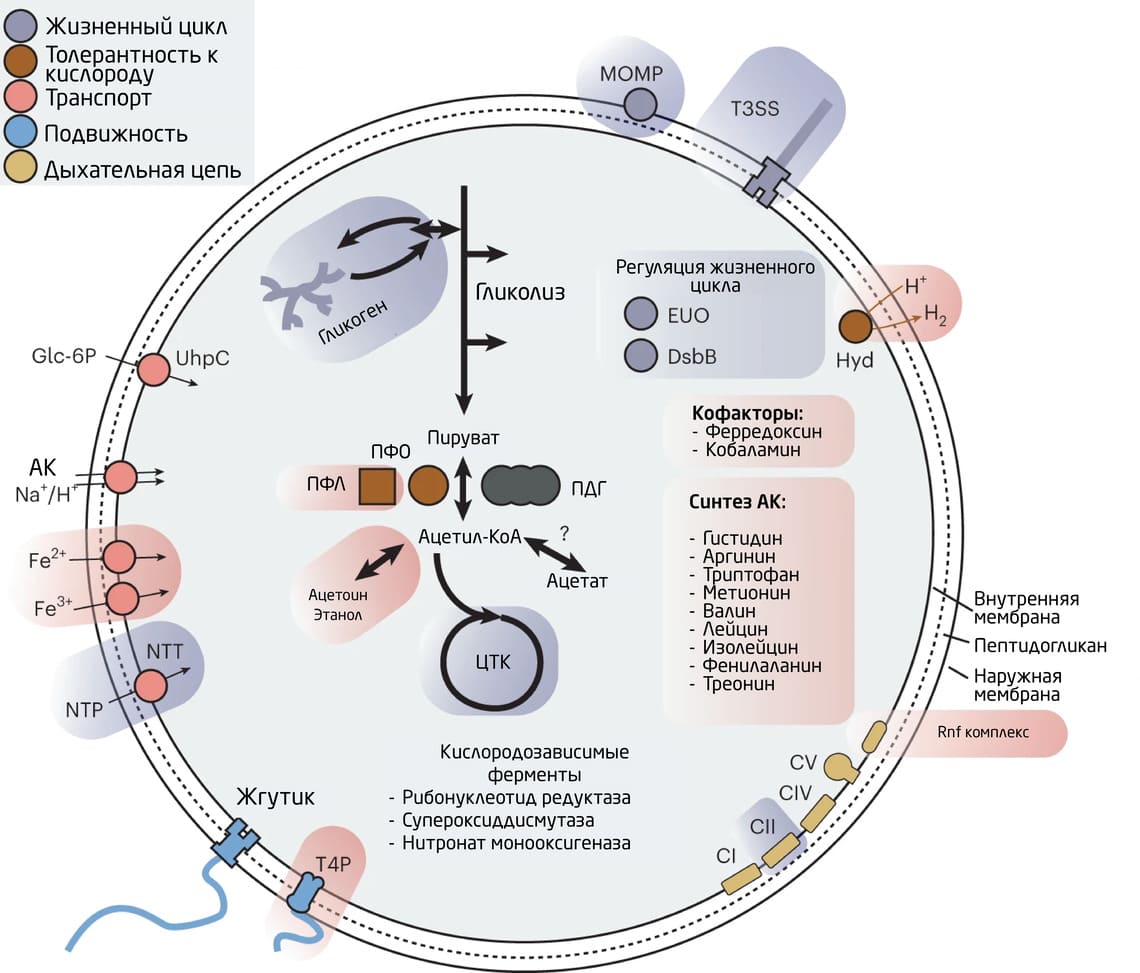
Рис. 1. Приобретение (синий фон) и потери (оранжевый фон) функциональных белков и соответствующих генов у последнего общего предка хламидий по сравнению с последним общим предком Chlamydiae, Verrucomicrobia, Lentisphaerae и Kiritimatiellaeota. Клеточная стенка на основе пептидогликана находится между внутренней и внешней мембранами. ПДГ – пируватдегидрогеназа; ПФО – пируват: ферредоксин-оксидоредуктаза; ПФЛ – пируват формат-лиаза; T4P – пили IV типа; MOMP – главный белок наружной мембраны; T3SS – III тип секреторной системы (инжектосома); Hyd – [FeFe]-гидрогеназа; Rnf– мембраносвязанный фермент простой дыхательной цепи, проявляет АТФ-азную активность, участвует в окислении и восстановлении NAD, действует как молекулярный насос и переносчик Na; CI–V – комплексы электрон-транспортной цепи I–V; АК – аминокислоты; NTT – транспортеры нуклеотидов; NTP – нуклеозидтрифосфаты; ЦТК – цикл трикарбоновых кислот; EUO – белок-репрессор транскрипции, избирательно регулирует промоторы генов и участвует в контроле экспрессии поздних генов (гены структурных вирусных белков); DsbB – белок B образования дисульфидной связи, элемент дыхательной цепи (участвует в переносе электронов от восстановленного белкового субстрата к молекулярному кислороду)
5.
Позднее хламидии разделились на 2 группы, G1 и G2, которые различались по степени толерантности к кислороду. Первые жили преимущественно в бескислородной среде, вторые – в кислородсодержащей. В группу G2 входили типичные патогены животных порядка Chlamydiales и бактерии порядка Amoebachlamydiales, инфицирующие простейших. Генетические различия в энергетическом метаболизме и аэробиозе (метаболические реакции в присутствии кислорода) между современными представителями Chlamydiae возникли гораздо позже 9, 10. У эндосимбионтов простейших наряду с увеличением размера генома в целом повышалось число генов, обеспечивающих более «гибкий» метаболизм, например, генов комплекса дыхательной цепи переноса электронов. Образ жизни общего предка, вероятно, включал переходы между кислородной и бескислородной средой.
Эволюция хламидий – наглядный пример перехода свободноживущих микроорганизмов к эндосимбиозу. Филогеномный анализ позволил реконструировать ключевые особенности генома предка Chlamydiae, подвижного факультативного анаэроба, способного инфицировать клетки эукариот. Вопреки ожидаемому «упрощению» генома и исключению лишних генов, переход от свободноживущих к симбиотическим формам сопровождался увеличением количества генов, метаболического потенциала и сложности организации бактерий.
Литература
1. Borges Á.H. et al. Chlamydia trachomatis vaccine development – a view on the current challenges and how to move forward. Expert Review of Vaccines. Taylor & Francis, 2022.
2. Kamneva O.K. et al. Analysis of Genome Content Evolution in PVC Bacterial Super-Phylum: Assessment of Candidate Genes Associated with Cellular Organization and Lifestyle. Genome Biology and Evolution, 2012.
3. Ishida K. et al. Amoebal Endosymbiont Neochlamydia Genome Sequence Illuminates the Bacterial Role in the Defense of the Host Amoebae against Legionella pneumophila. PLOS ONE, 2014.
4. Arthofer P. et al. Defensive symbiosis against giant viruses in amoebae. Proceedings of the National Academy of Sciences, 2022.
5. Dharamshi J.E. et al. Gene gain facilitated endosymbiotic evolution of Chlamydiae. Nature Microbiology, 2023.
6. Sevigny J.L. et al. Marker genes as predictors of shared genomic function. BMC Genomics, 2019.
7. Johnson J.S. et al. Evaluation of 16S rRNA gene sequencing for species and strain-level microbiome analysis. Nature Communications, 2019.
8. Gong W., Marchetti A. Estimation of 18S Gene Copy Number in Marine Eukaryotic Plankton Using a Next-Generation Sequencing Approach. Frontiers in Marine Science, 2019.
9. Wang Y. et al. Four superoxide dismutase (isozymes) genes of Bacillus cereus. Annals of Microbiology, 2011.
10. Englesberg E. et al. Some Enzymatic Changes Accompanying the Shift from Anaerobiosis to Aerobiosis in Pasteurella Pestis1. Journal of Bacteriology, 1954.




.jpg)























