- Главная страница
- Медиатека
- Статьи
- Разделяй и властвуй: 5 мифов о сортировке клеток: поддержка компании «Хеликон»
Медиатека
Разделяй и властвуй: 5 мифов о сортировке клеток
За годы работы с направлением клеточного сортинга мы столкнулись с целым ворохом всевозможных мифов и легенд, связанных с выбором оборудования для сортировки, и теперь готовы со всей серьезностью их развенчать.
Миф №1: Сортировка клеток – лучший способ выделения целевых клеток из гетерогенных популяций.
Сегодня есть три основные задачи, которые пользователи ставят перед клеточными сортерами: обогащение, выделение редких популяций и сортировка единичных клеток. И хотя сортер в этом отношении, действительно, и швец, и жнец, и на дуде игрец, далеко не всегда его использование является оптимальным решением. Вы же не будете покупать Порше, чтобы кататься на нем в соседний магазин?
Например, обогащение клеточной популяции – задача несложная, и решается простыми клеточными сепараторами и специальными реагентными наборами. А если говорить о таком тонком и деликатном деле, как работа с единичными клетками, то существует целый отдельный класс приборов, заточенный на эффективное решение именно таких задач.
Если вы не уверены в том, какой метод лучше всего подойдет для вашей работы, всегда можно написать нашим специалистам. Мы подберем решение, которое действительно необходимо: не больше и не меньше.
Миф №2: Чем больше лазеров, тем больше флуоресцентных каналов.
Классическое заблуждение, культивируемое производителями в самых разных областях: от мобильных телефонов до научных приборов (мы уже писали о том, как на самом деле связано количество пикселей с качеством изображения в гель-документирующих системах). Интерес производителя здесь очевиден: чем больше, тем дороже.
На самом деле, зачастую у сортеров с одними и теми же лазерами количество флуоресцентных каналов драматически различается. Все потому, что число каналов напрямую зависит от того, как физически расположены лазеры в приборе. В сортерах с коллинеарными лазерами количество флуоресцентных каналов гораздо меньше, чем в сортерах с лазерами, разделенными в пространстве, т.к. во втором случае сигнал от каждого лазера детектируется отдельно.
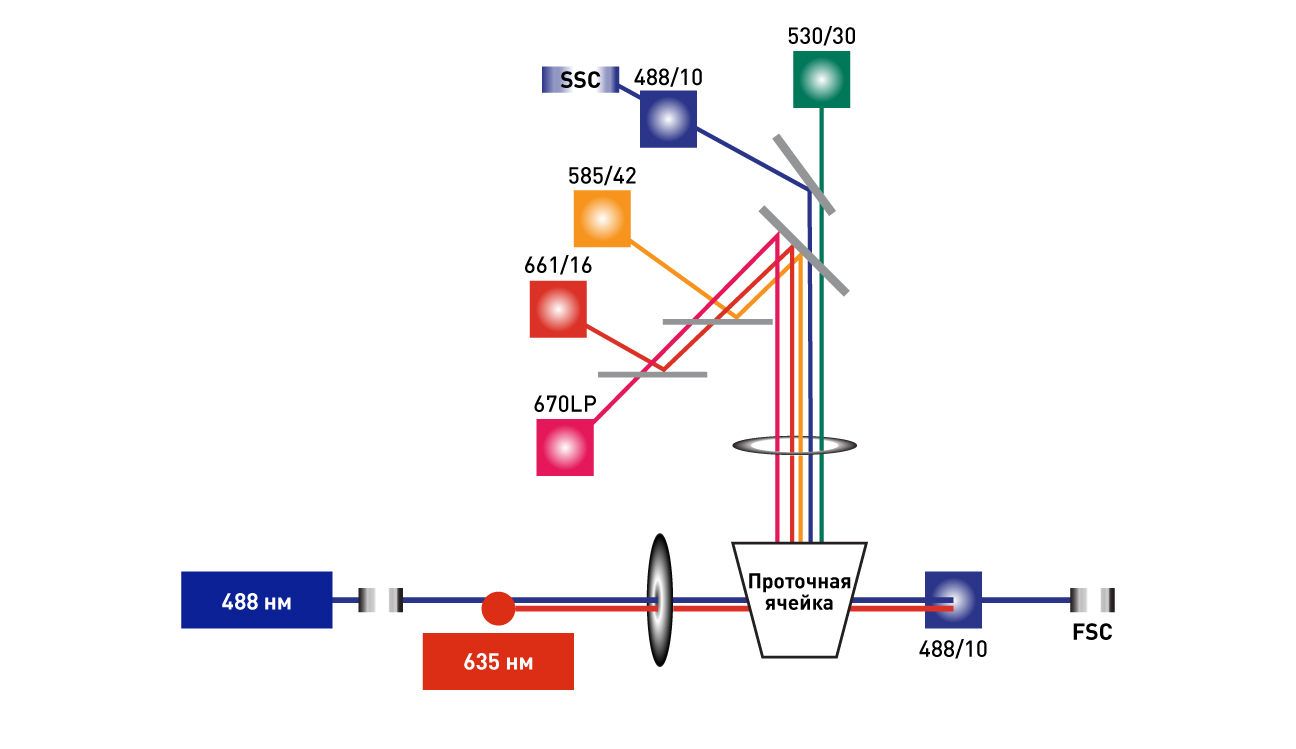
Рис.1 Оптическая схема с коллинеарными лазерами – 4 флуоресцентных канала.
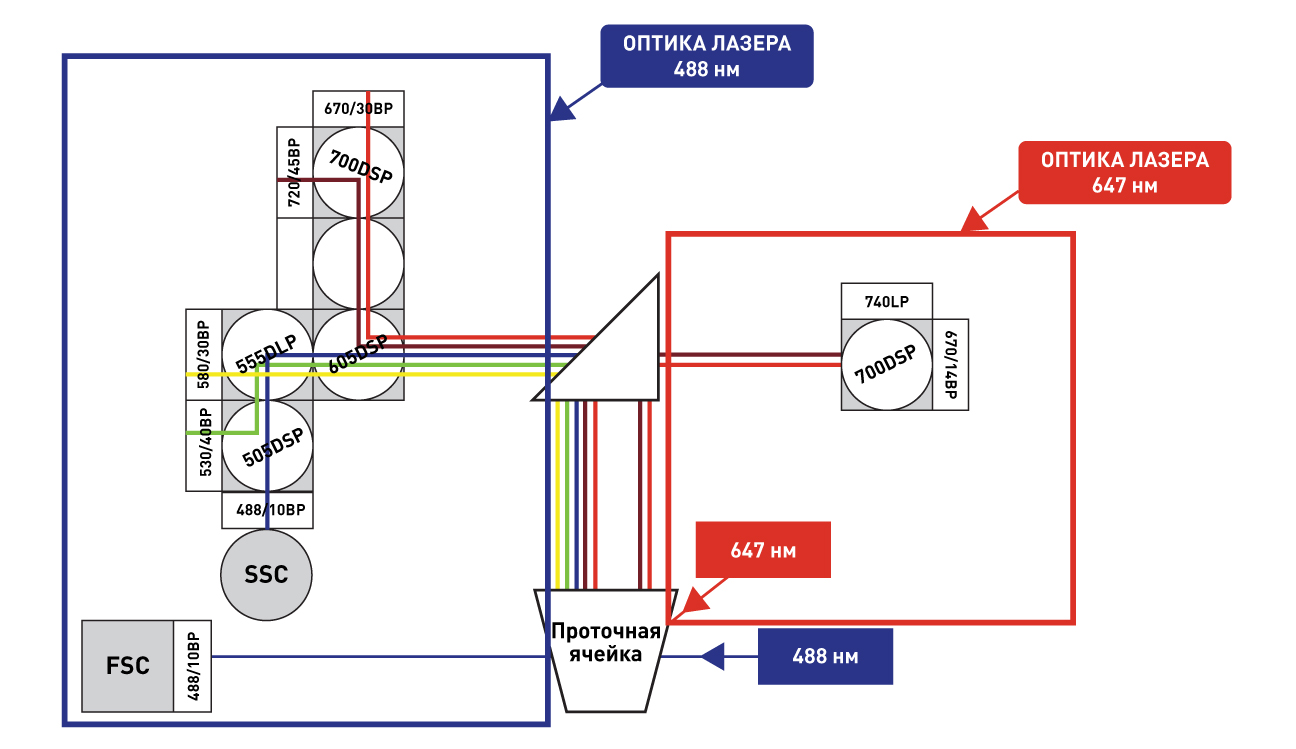
Рис.2 Оптическая схема с пространственно разделенными лазерами – 7 флуоресцентных каналов.
Миф №3: Максимальная скорость сортировки – это та скорость, с которой вы будете сортировать.
Реальность куда прозаичнее: максимальная скорость сортировки клеток – это та скорость, на которой можно сортировать калибровочные частицы при настройке сортера. Сортировка реальных клеток на таких скоростях приведет к значительному росту коэффициента вариации (CV) и падению чистоты сорта.
Такой расклад приемлем, когда стоит задача обогащения, но для обогащения есть более простые и гуманные способы (см. Миф №1). Во всех остальных случаях действительно важным является параметр чистоты сорта на заданной скорости. И вот здесь идет война за каждый лишний процент, особенно когда речь идет о редких популяциях – кто знает, не попадет ли ваша драгоценная клетка в тот самый 1%?
Миф №4: Одноразовые элементы жидкостного тракта – перспектива для клинического использования сортера клеток.
Один из самых активно распространяемых мифов, связанный с давней мечтой ученых и клиницистов использовать сортировку клеток для лечения пациентов, которую подогрел недавно вышедший .
К сожалению, этой мечте пока не суждено стать реальностью. Подавляющее большинство клеточных сортеров мирового рынка работают на технологиях, основанных на фокусировании клеток в потоке жидкости через систему капилляров. Это значит, что для гарантии стерильности и отсутствия кросс-контаминации весь жидкостной тракт сортера, от пробозаборника до системы сбора образца, должен быть сменным и одноразовым.
Некоторыми производителями оборудования, действительно, предпринимались попытки внедрения отдельных одноразовых элементов (например, использование сменного чипа вместо сопла), но в большинстве своем жидкостной тракт сортера до сих пор остается стационарными и требует стандартных процедур очистки. Это исключает возможность получения такими сортерами IVD сертификата за рубежом и регистрации в Минздраве РФ.
Продолжаем ждать и надеяться!
Миф №5: Чем выше чувствительность в эквивалентах (MESF), тем лучше качество сигнала.
Чувствительность в эквивалентах – это важно и хорошо. Но нужно иметь в виду, что не только MESF влияет на качество сигнала. Откровенно говоря, реальная разница между 115 и 125 MESF не так уж велика, так как большинство эпитопов содержатся в клетке в достаточном количестве, чтобы не замечать этой разницы. Кроме того, на одном антителе, как правило, связано больше одной молекулы флуорохрома, что позволяет успешно детектировать эпитопы в низких концентрациях.
Не менее важным параметром является разрешение сигнала. А разрешение зависит не только от чувствительности детекторов, но и от самой метки, от уровня автофлуоресценции объекта, от мощности лазера (чем мощнее лазер, тем больше сигнал с флуорохрома) и т.д. Как правило, в технических описаниях сортеров разрешение никак не цифруется, и единственный способ оценить этот параметр – по графикам сортировки флуоресцентных калибровочных частиц, которые часто приводят в рекламных материалах к приборам.
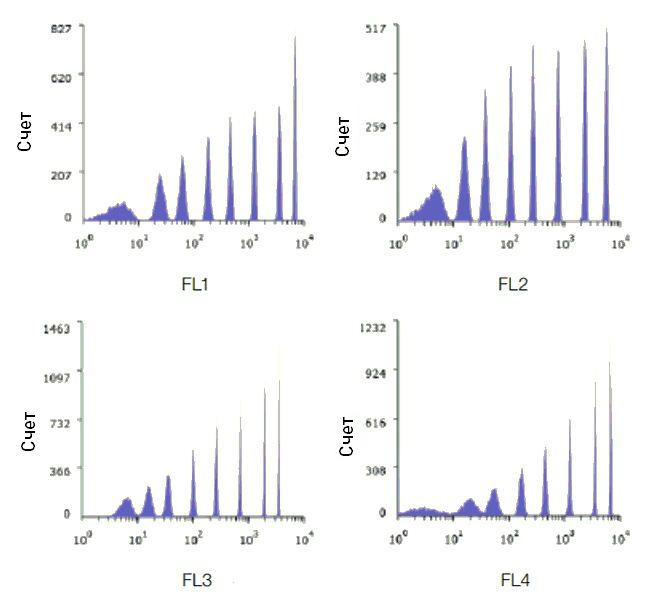
Рис.3 Пример детектирования флуоресцентных микросфер на сортере клеток. CV <2.5. Восемь пиков видны во всех 4-х флуоресцентных каналах.
Остались вопросы? Давайте обсудим! Напишите нам на электронную почту mail@helicon.ru.




.jpg)